Уроки по неорганической химии для подготовки к егэ
Содержание:
- Виртуальные лаборатории
- Пример 2
- Применение органических веществ
- Химические реакции (ОВР, химическое равновесие, скорость реакции и т.п.)
- Какой учебник по химии лучше
- PĀRTA
- Советы для подготовки к ЕГЭ по химии
- Составьте план
- Выберите наставника
- Определите ресурсы для подготовки к ЕГЭ
- Изучите спецификацию КИМ по предмету
- Внимательно читайте задания тестовой части
- Изучите критерии оценивания заданий части 2
- Не читайте узкоспециализированную литературу
- Научитесь работать с непрограммируемым калькулятором
- Проверяйте свои знания
- Строение атома и периодический закон
- Важнейшие классы неорганических веществ (оксиды, кислоты, основания, соли)
- Основные понятия и законы химии
- Бесплатно
- «ЕГЭ-студия»
- Что такое равновесие?
- Теория к заданию 11 из ЕГЭ по химии
- Классификация неорганических веществ с примерами соединений
Виртуальные лаборатории
Российский портал, на котором эксперименты из школьной программы можно смоделировать онлайн.
Международный ресурс, которые разрабатывают учёные со всего мира. Позволяет ставить более серьёзные опыты.
Проект по доставке на дом наборов для экспериментов. Также на сайте есть подробные и корректные инструкции по выполнению опытов. Многие ингредиенты для этих опытов можно самостоятельно купить в аптеке или продовольственном магазине. В дополнение к опытам на Mel Science полезно смотреть видео, которые объясняют суть химических явлений.

На портале есть множество полезных статей, подробные разборы опытов, инструкции, как проводить их в домашних условиях и где брать для них реактивы.
Пример 2
Установите соответствие между видом воздействия на равновесную систему и направлением смещения химического равновесия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
NH3(г) + H2O(ж) ⇄ NH4+(р-р) + OH—(р-р)
| ВОЗДЕЙСТВИЕА) добавление хлорида калияБ) повышение давленияВ) добавление катализатораГ) добавление твердой щелочи | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ1) в сторону прямой реакции2) в сторону обратной реакции3) практически не смещается |
Решение
Начнем с уже привычных нам давления и катализатора. Катализатор не влияет на смещение равновесия (ответ 3), а повышение давления смещает равновесие в сторону меньшего количества газов, то есть в сторону прямой реакции (ответ 1).
Теперь обратимся к варианту А. Хлорид калия – растворимое вещество, значит, в растворе будет диссоциировать на ионы калия и хлорид-ионы. Но ни те, ни другие не будут взаимодействовать с нашими участниками реакции. Следовательно, KCl не влияет на равновесие системы.
В варианте Г нам предлагают рассмотреть добавление твердой щелочи. Здесь легко попасть в ловушку, ведь твердые вещества не смещают равновесие. Но не стоит забывать, что любая щелочь – это растворимое основание, а значит, она продиссоциирует в водном растворе на ионы Н+ и ОН—, тем самым увеличивая концентрацию гидроксид-ионов. А при увеличении продуктов реакции равновесие смещается в сторону обратной реакции — ответ 2.
Так мы получили ответ 3132.
Как видите, задание 24 ЕГЭ по химии не стало сложнее! Для его успешного выполнения вам необходимо вспомнить принцип Ле Шателье, а также обратить внимание на растворимость твердых веществ, если они присутствуют. Если хотите разобраться с остальными темами, обязательно приходите к нам на бесплатную консультацию
И удачи в подготовке!
Применение органических веществ
Органические вещества – это класс химических соединений, объединяющий все вещества, в состав которых входит углерод.
Алканы
Предельные (насыщенные) углеводороды, атомами водорода: СН4 – метан (основа природного газа), С2Н6 – этан, С3Н8 – пропан, С8Н18 – октан (основа бензина).
- Применяются в качестве топлива: бензин, дизельное, авиационное, пропан-бутановая смесь для бытовых плит.
- Вазелин – незаменим в медицине, парфюмерии, косметологии.
- Входят в состав смазочных масел.
- Хладагент для холодильников.
- Петролейный эфир и циклогексан используются в качестве растворителя.
- Метан незаменимый компонент при производстве шин.
Широко распространено применение данной группы органических соединений в химической промышленности (для производства пластмасс, синтетических волокон и т.д.) и медицине.
Алкены
Соединения служат исходными веществами для получения ряда готовых продуктов:
- растворителей (спиртов, дихлорэтана, эфира);
- полимеров (полиэтилена, поливинилхлорида, полиизобутилена);
Этилен (Н2С=С Н2) используется для получения, тефлона, этилового спирта, уксусного альдегида, галогенопроизводных и многих других органических соединений.
Алкены применяются и для ускорения процесс созревания фруктов.
Алкины (ацетиленовые углеводороды)
Ацетилен – необходим в качестве исходного продукта в органическом синтезе при производстве:
- полимеров (каучука, поливинилхлорида и др.);
- растворителей (1,1,2,2-тетрахлорэтана , 1,1,2-трихлорэтена);
- уксусной кислоты.
Температура пламени вещества достигает 3150°С, что нашло свое применение при резке металла и в сварке.
Спирты
Алкоголи – производные углеводородов, в которых один или несколько атомов водорода замещены на гидроксильную группу ОН.
Метанол (СН3ОН) –применяется в производстве муравьиной кислоты и формальдегида. Рассматривается как вариант для применения в качестве моторного топлива.
Этанол (С2Н5ОН)- востребован в виде исходного соединения для получения уксусной кислоты, сложных эфиров, карбоновых кислот. Вещество служит основой производства спиртосодержащей продукции и антисептических средств.
Этиленгликоль – компонент необходимый в производстве пластмасс, антифризов, органическом синтезе.
Глицерин – незаменим в разных отраслях промышленности, в том числе текстильной, пищевой, фармакологии.
Фенолы
Основное использование соединений приходится на химическую промышленность, медицину (производство синтетических смол, красителей, антисептиков, взрывчатых веществ и т.д.).
Альдегиды
Метаналь – используется при получении фенолформальдегидных и карбамидных смол, синтезе лекарственных средств, как дезинфицирующее средство.
Этаналь — нашел свое применение в органическом синтезе.
Карбоновые кислоты
Соединения, карбоксильной группы –СООН.
Муравьиная кислота (НСООН) –применяется в фармацевтической и пищевой промышленности. Уксусная кислота (СН3СООН) — востребована для производства искусственных волокон на основе целлюлозы и в пищевой промышленности.
Бензойная кислота (С6Н5СООН) – незаменима в фармацевтике для синтеза душистых веществ и красителей, а также в качестве консерванта для пищевых продуктов.
Сложные эфиры
Применяются в пищевой и парфюмерной отраслях в качестве отдушек. А также обеспечивают эластичность и пластичность пластмасс и резины.
Также широко распространено в пищевой промышленности, медицине применение глюкозы, аминов, аминокислот. Целлюлоза основной компонент при изготовлении бумаги, пленок, искусственных волокон и т.д.
Много соединений еще не изучено до конца, и возможно, благодаря науке человек сможет заменить натуральные продукты на искусственные, органических соединений природного происхождения применяется все меньше.
Смотри также:
- Понятие о металлургии: общие способы получения металлов
- Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия
- Природные источники углеводородов, их переработка
- Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки
Химические реакции (ОВР, химическое равновесие, скорость реакции и т.п.)
Тесты и задания с видео-объяснением:
- Тесты по теме Химические реакции. Часть 1
- Тесты по теме Химические реакции. Часть 2
- Тесты по теме Химические реакции. Часть 3
- Тесты по теме Химические реакции. Часть 4
- Тесты по теме Химические реакции. Часть 5
Тесты и задания без видео-объяснения (с ответами):
- Тест по теме Химические реакции
- Окислительно-восстановительные реакции. Часть 1
- Окислительно-восстановительные реакции. Часть 2
- Окислительно-восстановительные реакции. Часть 3
- Окислительно-восстановительные реакции. Часть 4
- Классификация химических реакций в неорганической и органической химии. Часть 1
- Классификация химических реакций в неорганической и органической химии. Часть 2
- Скорость химической реакции, её зависимость от различных факторов. Часть 1
- Скорость химической реакции, её зависимость от различных факторов. Часть 2
- Реакции окислительно-восстановительные. Окислители и восстановители. Часть 1
- Реакции окислительно-восстановительные. Окислители и восстановители. Часть 2
- Электролиз растворов и расплавов. Часть 1
- Электролиз растворов и расплавов. Часть 2
- Химическое равновесие. Часть 1
- Химическое равновесие. Часть 2
Какой учебник по химии лучше
На основе сравнения достоинств, недостатков, актуальности информации, наличия гдз команда ВыборЭксперта.ру выбрала 4 издания для подготовки к экзаменам и углубления знаний по химии:
- Для изучения азов подойдёт учебник 8 класса Габриелян.
- Начала органики кратко и интересно описаны в учебнике 9 класса Рудзитис.
- Если нужен профильный учебник химии, рекомендуем материалы Ерёмина за 11 класс.
- Вдогонку к учебнику возьмите углублённый справочник Ерёмина для отработки и повторения теории.
Основываясь на критериях выбора, наших рекомендациях, составьте личный список литературы. Указанных книг достаточно для освоения общей, неорганической и органической химии на профильном уровне.
PĀRTA

Сайт:; https://vk.comСтоимость: пробный урок — бесплатно, от 2990 р./мес.
- Выпустили 6 стобалльников и 34+ ученика на 90+ баллов в 2020 году (только по химии)
- Бесплатный вебинар каждое воскресенье (тестовая часть и задания повышенной сложности)
- Сотрудничают с экспертом по подготовке к ЕГЭ
- Объясняют сложное простым языком
Подготовка к экзамену по химии проводится в формате мастер-группы. Преподаватель и куратор сами сдали ЕГЭ на высший балл и готовы помочь своим ученикам добиться топовых результатов.
В программе обучения (на тарифе Лайт):
- 16 занятий в месяц по 1,5-2 часа
- Домашняя работа с проверкой и разбором ошибок
- Личный ментор
- Беседа с другими учениками
- Входной тест
- Скрипты и конспекты к урокам
- Авторские документы от преподавателей
Доступно 3 тарифа на выбор:
- ЛАЙТ (описание выше)
- МЕДИУМ: тариф Лайт + Вебинар с экспертом ЕГЭ, курс экстра-повторение, зачёт и пробник
- ХАРД: тариф Медиум + Банк заданий, секретный канал с твоим преподавателем в Telegram, система жизней
Советы для подготовки к ЕГЭ по химии
Составьте план
Например, каждую неделю в понедельник и среду два часа вы занимаетесь химией. Кроме того, вы можете воспользоваться нашим планером для подготовки. Записывайте в нём главные задачи дня и вопросы учителю, а также что нового вы узнали, какие темы прошли и какие ещё предстоит разобрать, что нужно поискать дополнительно.
Выберите наставника
Найдите человека, который сможет ответить на все возникающие вопросы. Это может быть учитель или знакомый студент, изучающий химию.
Определите ресурсы для подготовки к ЕГЭ
Это и печатные материалы, и электронные образовательные ресурсы. Помните, что ЕГЭ периодически меняют, и не все пособия могут быть актуальными, даже если выпущены в текущем году. Среди популярных ресурсов для подготовки к экзамену по химии:
- Д.Ю. Добротин, «Методические рекомендации обучающимся по организации индивидуальной подготовки к ЕГЭ. Химия», ФИПИ, Москва, 2020 г;
- В.Н. Доронькин и др. «ЕГЭ. Химия. Тематический тренинг. Задания базового и повышенного уровня сложности» Легион, Ростов-на Дону, 202_г.;
- В.Н. Доронькин и др. «ЕГЭ. Химия. Тематический тренинг. Задания высокого уровня сложности» Легион, Ростов-на Дону, 202_г.;
- Д.Ю. Добротина «ЕГЭ. Химия. Типовые экзаменационные варианты», Национальное образование, М, 202_г.;
- Е.В. Зыкова «Сборник задач и упражнений по органической химии» Феникс, Ростов-на Дону, 2019г.;
- Сайт ФИПИ;
- Образовательный портал «РЕШУ ЕГЭ»;
- Сайт «Наука для тебя».
Изучите спецификацию КИМ по предмету
Актуальная информация есть на сайте ФИПИ. Изучайте сначала теорию по каждому вопросу. Помните, что информации из школьного учебника может быть недостаточно. Выполняйте тематические тесты и только потом общие варианты ЕГЭ.
Внимательно читайте задания тестовой части
Не трактуйте тексты задач, основываясь на личных ассоциациях или опыте решения аналогичных заданий. Отвечайте на поставленный вопрос. Например, если вас просят записать ответ с точностью до десятых, не нужно записывать получившееся число полностью. Если просят выписать числа, соответствующие кислоте и щелочи, пишите только в той последовательности, которая соответствует кислоте и щелочи, а не наоборот
Особое внимание нужно обращать и на количество требуемых ответов к заданиям. С 2021 года в заданиях 19 и 20 предлагается выбрать все верные ответы
Их может быть два, три или четыре.
Изучите критерии оценивания заданий части 2
За правильно решенное, но неправильно оформленное задание вы можете потерять баллы. При этом некоторые нюансы знают только эксперты ЕГЭ
Например, необходимо обратить внимание, что если в задании №30 (ОВР) допустимо использовать удвоенные коэффициенты в уравнениях реакций, то в сокращенном ионном уравнении (задание №31) удвоенные коэффициенты недопустимы. Или, если ранее в задании №30 была допустима форма записи:
2Cl+2e=2Cl— 1 восстановление, окислитель;
то сейчас:
2Cl+2e=2Cl— 1 окислитель, восстановление;
т.е. окислитель и восстановитель (можно даже проставить просто буквы О или В) пишутся только спереди (допустимы и другие формы записи).
Если в задании №30 для некоторых химических элементов допустимо поставить и степень окисления, и заряд (S-2 и S2-), то для других элементов этого делать категорически нельзя (N+3, но не N3+, т.к. такой частицы реально не существует).
В задании №33 необходимо обратить внимание, как функциональные заместители или катализаторы влияют на направление химической реакции. Сравните, например, галогенирование алканов на свету и в жестких условиях; гидрогалогенирование несимметричных алкенов при нормальных условиях и в присутствии катализатора H2O2
Не читайте узкоспециализированную литературу
Во-первых, это отнимает время. Во-вторых, помните, что ЕГЭ проверяет школьные знания — они не всегда соответствуют современной науке.
Научитесь работать с непрограммируемым калькулятором
Помните: когда вы считаете в телефоне, он правильно проводит порядок действий. При работе с калькулятором порядок действий вам придется соблюдать самостоятельно. Посчитайте ради интереса в телефоне и на калькуляторе простейший пример: 2+2*2. Сравните ответы.
Проверяйте свои знания
Периодически проверяйте уровень усвоения как новых, так и ранее полученных знаний. Тематические тесты или полные варианты ЕГЭ вы можете найти на сайте ФИПИ. Подготовка к ЕГЭ 2021 по химии будет проще, если под рукой будут все необходимые материалы. Зарегистрируйтесь на нашем сайте и получите доступ к библиотеке полезных материалов для подготовки.
Строение атома и периодический закон
Тесты и задания с видео-объяснением:
- Тесты по теме Строение атома и периодический закон. Часть 1
- Тесты по теме Строение атома и периодический закон. Часть 2
- Тесты по теме Строение атома и периодический закон. Часть 3
- Тесты по теме Строение атома и периодический закон. Часть 4
- Тесты по теме Строение атома и периодический закон. Часть 5
- Тесты по теме Строение атома и периодический закон. Часть 6
Тесты и задания без видео-объяснения (с ответами):
- Электронная конфигурация атома. Часть 1
- Электронная конфигурация атома. Часть 2
- Закономерности изменения химических свойств элементов. Характеристика элементов. Часть 1
- Закономерности изменения химических свойств элементов. Характеристика элементов. Часть 2
Важнейшие классы неорганических веществ (оксиды, кислоты, основания, соли)
Тесты и задания с видео-объяснением:
- Тесты по теме Основные классы неорганических веществ. Часть 1
- Тесты по теме Основные классы неорганических веществ. Часть 2
- Тесты по теме Основные классы неорганических веществ. Часть 3
- Тесты по теме Основные классы неорганических веществ. Часть 4
- Тесты по теме Основные классы неорганических веществ. Часть 5
- Тесты по теме Основные классы неорганических веществ. Часть 6
- Тесты по теме Основные классы неорганических веществ. Часть 7
- Тесты по теме Основные классы неорганических веществ. Часть 8
- Тесты по теме Основные классы неорганических веществ. Часть 9
Тесты и задания без видео-объяснения (с ответами):
- Тест по теме Классы неорганических веществ
- Классификация и номенклатура неорганических веществ. Часть 1
- Классификация и номенклатура неорганических веществ. Часть 2
Основные понятия и законы химии
Тесты и задания с видео-объяснением:
- Тесты по теме Основные понятия и законы химии. Часть 1
- Тесты по теме Основные понятия и законы химии. Часть 2
- Тесты по теме Основные понятия и законы химии. Часть 3
- Тесты по теме Основные понятия и законы химии. Часть 4
- Тесты по теме Основные понятия и законы химии. Часть 5
- Тесты по теме Основные понятия и законы химии. Часть 6
- Тесты по теме Основные понятия и законы химии. Часть 7
Тесты и задания без видео-объяснения (с ответами):
- Электроотрицательность, степень окисления и валентность химических элементов. Часть 1
- Электроотрицательность, степень окисления и валентность химических элементов. Часть 2
Бесплатно
CHEMEGE.RU

Сайт: https://chemege.ru
На сайте вы найдете полный теоретический курс подготовки к ЕГЭ по химии-2021. Приведена теория по каждому заданию в соответствии с кодификатором.
К части тем есть тренировочные тесты и задачи. Также есть раздел с видеоопытами по общей, неорганической и органической химии.
ЕГЭ.рф

Сайт: https://егэ.рф
Сайт предоставляет шанс всем желающим пройти ЕГЭ по химии для оценки текущего уровня подготовки. Тестирование проводится онлайн на реальных вариантах ЕГЭ. Платформа сотрудничает с ФИПИ.
Тестовую часть проверяет компьютер, результат будет доступен сразу. Письменную часть можно отправить на проверку реальному эксперту ЕГЭ. Стоимость услуги: 500 р. — оценка письменной части без комментариев, 1000 р. — с развернутыми комментариями эксперта.
«4ЕГЭ»

Сайт: https://4ege.ru
Здесь вы найдете материалы для подготовки к ЕГЭ по химии по разным темам:
- Видеоразборы отдельных заданий в ЕГЭ по химии
- Методические пособия с теорией
- Записи вебинаров по теоретическим темам
- Шпаргалки для запоминания
«Синергия»

Сайт: https://synergy.ru
На сайте собраны все актуальные материалы по теме ЕГЭ по химии:
- Демоверсии и КИМы за 2021 год
- ЕГЭ предыдущих периодов (2019-2020)
- Теоретическая часть: по каждому типу заданий ЕГЭ, а также химия в схемах и таблицах, таблица Менделеева, таблица растворимости
- Практическая часть: подборка задач по каждому типу заданий ЕГЭ с ответами для самопроверки
«РешуЕГЭ»

Сайт: https://chem-ege.sdamgia.ru
Это сайт-тренажер, где каждый месяц появляются новые варианты тренировочных заданий по химии: тестовой части и с развернутым ответом. Варианты генерируются компьютером: из новых заданий и самых сложных заданий по статистике прошлого месяца.
Чтобы проверить свои знания по определенному разделу химии, можно сформировать тест самостоятельно — из каталога заданий по интересующим вас темам.
Яндекс.Репетитор
Сайт: https://yandex.ru
Здесь вы найдете 6 видео-уроков по 45 минут по темам:
- Решение расчетных задач
- Классификация неорганических веществ. Химические свойства основных классов неорганических веществ
- Окислительно-восстановительные реакции. Электролиз
- Химические реакции. Скорость химической реакции. Химическое равновесие
- Строение вещества
- Строение атома. Периодический закон
Также здесь можно порешать тесты. Варианты похожи на те, что используются на реальном ЕГЭ, потому что их составляют эксперты, в том числе авторы «СтатГрада». Каталог заданий регулярно обновляется.
«Птичка Химичка -Химия с Нуля-«

Сайт: https://www.youtube.com
Автор канала обещает помочь всем желающим разобраться в химии.
Здесь собраны видео по разным темам:
- Что нужно знать для ЕГЭ
- Актуальная информация по ЕГЭ 2021
- Полный курс химии из 92 уроков
- 71 видео по теме: Общая химия. Понятия. Законы. Формулы
- Видео по отдельным темам: Органическая химия, Типы химических связей, Классы неорганических соединений, Неорганическая химия
Смотреть видео нужно подряд, не пропуская уроков, и результат не заставит себя ждать.
«examtop»

Сайт: https://www.youtube.com
На канале выходят видеоуроки для подготовки к ЕГЭ по химии с доп. материалами и актуальными заданиями 2021 года.
В плейлистах собраны уроки по темам:
- Курс: Задание 34 ЕГЭ по химии (на примерах реальных задач). 69 видео
- Курс: Органическая химия. Подготовка к ЕГЭ. 20 видео
- Курс: Неорганическая химия. Подготовка к ЕГЭ. 17 видео
- Видео-разборы отдельных заданий ЕГЭ по химии
«Химия ЕГЭ 2021 — АКАДЕМИЯ ЕГЭ N1»

Сайт: https://www.youtube.com
В бесплатном доступе 129+ видеоуроков с разборами заданий из ЕГЭ по химии и теорией к экзамену. В отдельном плейлисте собраны прямые трансляции с разбором заданий, полезными фишками и лайфхаками по подготовке. Новые уроки выходят 2 раза в неделю.
«ЕГЭ-студия»
Онлайн-курсы ЕГЭ по химии по авторской методике Лолиты Окольновой.
В программе:
- Качественный теоретический материал по всем темам ЕГЭ по химии, записи вебинаров
- 9 онлайн мастер-классов Лолиты Окольновой по всем темам ЕГЭ по химии по расписанию
- Подготовительные задания к каждому мастер-классу: задачи с видеоразбором (разбираем химию органических и неорганических веществ, химические реакции, проводим тесты)
- Полные видеозаписи всех мастер-классов
- Домашние задания, которые проверяют индивидуально лучшие репетиторы по химии
- Прогноз по задачам ЕГЭ-2021 от Лолиты Окольновой и аналитического отдела компании «ЕГЭ-Студия»
- 3 пробных ЕГЭ в течение учебного года с проверкой и полным видеоразбором
- Дополнительные мастер-классы с ведущими педагогами России
Доступно три варианта подготовки:
10 класс (готовься заранее)
- ДЗ с проверкой
- 4 занятия в месяц
11 класс на 75 баллов
- ДЗ с проверкой
- 4 занятия в месяц
- База знаний (теория и практика)
11 класс на 100 баллов
- ДЗ с проверкой
- 8 занятий в месяц
- База знаний (теория и практика)
Что такое равновесие?
Чтобы решить 24 задание ЕГЭ по химии, для начала вспомним, что такое равновесие и как его смещать.
Химическое равновесие — состояние химической системы, при котором скорость прямой реакции равна скорости обратной.
Записав уравнение химической реакции в тетради, мы можем понять, какое количество реагентов вступает в эту реакцию, какие продукты мы получаем. Но на практике превращения далеки от идеала. Вещества реагируют не полностью, образуются отходы, возникают потери. Смещение равновесия позволяет регулировать течение реакции так, как этого требует производственный процесс.
Мы будем сталкиваться с понятиями «смещение в сторону прямой реакции» или «в сторону продуктов». Это означает, что в результате реакции мы сможем получить больше продуктов, то есть увеличить выход.
«Смещение в сторону обратной реакции» или «в сторону реагентов» позволяет уменьшить выход продуктов, уменьшить их выход и тем самым увеличить выход обратной реакции.
В 1884 году французский химик Анри Ле Шателье сформулировал принцип, согласно которому, при воздействии на систему, находящуюся в состоянии равновесия (температура, давление, концентрация), система стремится компенсировать внешнее воздействие.
- При увеличении давления равновесие смещается в сторону меньших газов, при уменьшении давления — в сторону больших газов;
- При увеличении температуры равновесие смещается в сторону эндотермической реакции, при уменьшении — в сторону экзотермической реакции;
- При увеличении концентрации реагентов равновесие смещается в сторону продуктов реакции и наоборот.
Посмотрим, как в 2020 году изменили варианты ответов, сделав это задание «суперсложным» (на самом деле нет).
Самостоятельно подготовиться к ЕГЭ непросто. На то, чтобы разобраться со всеми темами, понадобится много времени. Но и это не решит проблему! Например, если вы запомнили какое-то решение из интернета, а оно оказалось неправильным, можно на пустом месте потерять баллы
Если хотите научиться решать все задания ЕГЭ по химии, обратите внимание на онлайн-курсы MAXIMUM! Наши специалисты уже проанализировали сотни вариантов ЕГЭ и подготовили для вас вас максимально полезные занятия.Приходите к нам на консультацию — вы сможете пройти диагностику по выбранным предметам ЕГЭ, поставить цели и составить стратегию подготовки, чтобы получить на экзамене высокие баллы. Все это абсолютно бесплатно!
Теория к заданию 11 из ЕГЭ по химии
Классификация органических соединений
Известно, что свойства органических веществ определяются их составом и химическим строением. Поэтому неудивительно, что в основе классификации органических соединений лежит именно теория строения — теория А. М. Бутлерова. Классифицируют органические вещества по наличию и порядку соединения атомов в их молекулах. Наиболее прочной и малоизменяемой частью молекулы органического вещества является ее скелет — цепь атомов углерода. В зависимости от порядка соединения атомов углерода в этой цепи вещества делятся на ациклические, не содержащие замкнутых цепей атомов углерода в молекулах, и карбоциклические, содержащие такие цепи (циклы) в молекулах.
Классификация органических веществ (по строению углеродной цепи молекул).
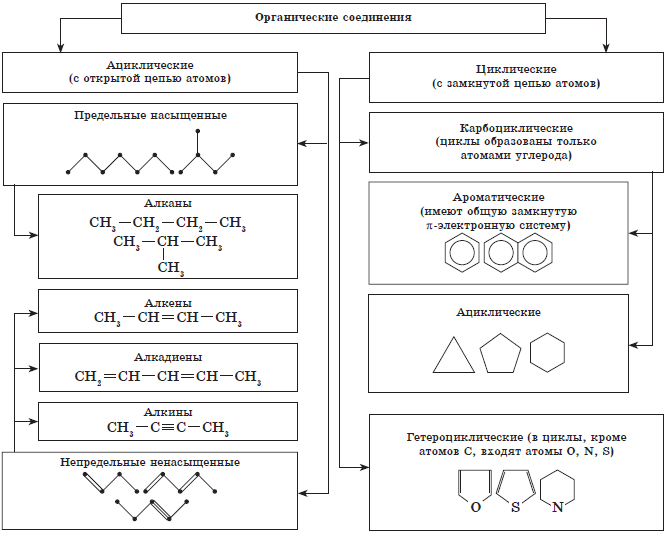
Помимо атомов углерода и водорода молекулы органических веществ могут содержать атомы и других химических элементов. Вещества, в молекулах которых эти так называемые гетероатомы включены в замкнутую цепь, относят к гетероциклическим соединениям.
Гетероатомы (кислород, азот и др.) могут входить в состав молекул и ациклических соединений, образуя в них функциональные группы, например, гидроксильную — $ОН$, карбонильную , карбоксильную — , аминогруппу — $NH_2$.
Номенклатура органических соединений
В начале развития органической химии открываемым соединениям присваивались тривиальные названия, часто связанные с историей их получения: уксусная кислота (являющаяся основой винного уксуса), масляная кислота (образующаяся в сливочном масле), гликоль (т.е. сладкий) и т.д. По мере увеличения числа новых открытых веществ возникла необходимость связывать названия с их строением. Так появились рациональные названия: метил амин, диэтиламин, этиловый спирт, метилэтилкетон, в основе которых лежит название простейшего соединения. Для более сложных соединений рациональная номенклатура непригодна.
Теория строения А. М. Бутлерова стала основой для классификации и номенклатуры органических соединений по структурным элементам и по расположению атомов углерода в молекуле. В настоящее время наиболее употребляемой является номенклатура, разработанная Международным союзом теоретической и прикладной химии (IUРАС), которая называется номенклатурой ИЮПАК. Правила ИЮПАК рекомендуют для образования названий несколько принципов, один из них — принцип замещения. На основе этого разработана заместительная номенклатура, которая является наиболее универсальной. Приведем несколько основных правил заместительной номенклатуры и рассмотрим их применение на примере гетерофункционального соединения, содержащего две функциональные группы, — аминокислоты лейцина:
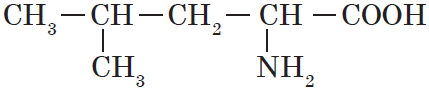
1. В основе названия соединений лежит родоначальная структура (главная цепь ациклической молекулы, карбоциклическая или гетероциклическая система). Название родоначальной структуры составляет основу названия, корень слова.
В данном случае родоначальной структурой является цепь из пяти атомов углерода, связанных одинарными связями. Таким образом, коренная часть названия — пентан.
2. Характеристические группы и заместители (структурные элементы) обозначаются префиксами и суффиксами. Характеристические группы подразделяются по старшинству. Порядок старшинства основных групп:
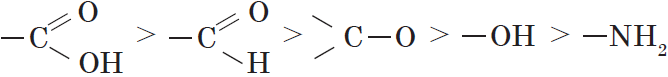
Выявляют старшую характеристическую группу, которую обозначают в суффиксе. Все остальные заместители называют в префиксе в алфавитном порядке.
В данном случае старшей характеристической группой является карбоксильная, т.е. это соединение относится к классу карбоновых кислот, поэтому к коренной части названия добавляем -овая кислота. Второй по старшинству группой является аминогруппа, которая обозначается префиксом амино-. Кроме этого, молекула содержит углеводородный заместитель метил-. Таким образом, основой названия является аминометилпентановая кислота.
3. В название включают обозначение двойной и тройной связи, которое идет сразу после корня. Рассматриваемое соединение не содержит кратных связей.
4. Атомы родоначальной структуры нумеруют. Нумерацию начинают с того конца углеродной цепи, к которому ближе расположена старшая характеристическая группа:
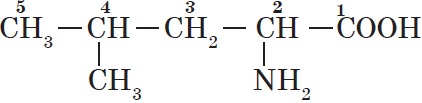
Нумерацию цепи начинают с атома углерода, входящего в состав карбоксильной группы, ему присваивается номер $1$. В этом случае аминогруппа окажется при углероде $2$, а метил — при углероде $4$.
Таким образом, природная аминокислота лейцин по правилам номенклатуры ИЮПАК называется $2$-амино-$4$-метилпентановая кислота.
Классификация неорганических веществ с примерами соединений
Как мы видим, прежде всего все неорганические вещества делятся на простые и сложные:
Простыми веществами называют такие вещества, которые образованы атомами только одного химического элемента. Например, простыми веществами являются водород H2, кислород O2, железо Fe, углерод С и т.д.
Среди простых веществ различают металлы, неметаллы и благородные газы:
Металлы образованы химическими элементами, расположенными ниже диагонали бор-астат, а также всеми элементами, находящимися в побочных группах.
Благородные газы образованы химическими элементами VIIIA группы.
Неметаллы образованы соответственно химическими элементами, расположенными выше диагонали бор-астат, за исключением всех элементов побочных подгрупп и благородных газов, расположенных в VIIIA группе:
Названия простых веществ чаще всего совпадают с названиями химических элементов, атомами которых они образованы. Однако для многих химических элементов широко распространено такое явление, как аллотропия. Аллотропией называют явление, когда один химический элемент способен образовывать несколько простых веществ. Например, в случае химического элемента кислорода возможно существование молекулярных соединений с формулами O2 и O3. Первое вещество принято называть кислородом так же, как и химический элемент, атомами которого оно образовано, а второе вещество (O3) принято называть озоном. Под простым веществом углеродом может подразумеваться любая из его аллотропных модификаций, например, алмаз, графит или фуллерены. Под простым веществом фосфором могут пониматься такие его аллотропные модификации, как белый фосфор, красный фосфор, черный фосфор.
